Estados de la materia
Los estados de la materia son las diversas formas en que se presenta la materia en el universo. Se conocen también como estados de agregación de la materia, ya que las partículas se agregan o agrupan de maneras diferentes en cada estado.
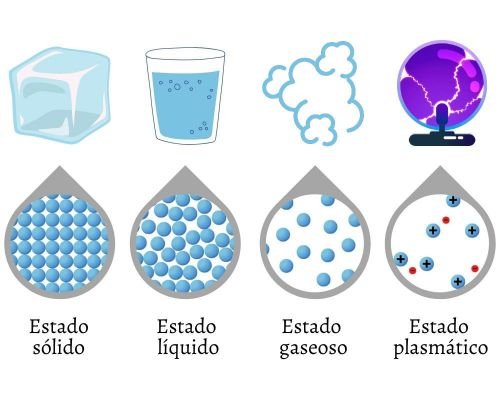
Se puede considerar que existen cuatro estados físicos y fundamentales de la materia, tomando en cuenta aquellas formas de agregación que se presentan bajo condiciones naturales. Los estados fundamentales de la materia son:
- Estado sólido.
- Estado líquido.
- Estado gaseoso.
- Estado plasmático.
Sin embargo, los estudios sobre los estados de agregación de la materia se han extendido en la actualidad. Además de aquellos que se presentan naturalmente, hoy se estudian aquellos que se presentan en condiciones extremas, inducidas en laboratorio. De este grupo, los científicos han comprobado la existencia de tres nuevos estados: el condensado de Bose-Einstein (BEC); el condensado de Fermi y el supersólido.
Las características de los estados de la materia dependen de la fuerza de atracción entre las partículas y su movilidad. La temperatura y/o la presión son los factores que afectan cómo se agrupan dichas partículas y cómo interactúan entre sí.
Cuando hay alteraciones sensibles en las variables de temperatura y/o presión, se producen cambios de un estado de la materia al otro. Estos cambios son solidificación, vaporización, fusión, sublimación, sublimación inversa, ionización y desionización.
A continuación, presentamos un cuadro comparativo con las principales características y diferencias que existen entre los estados fundamentales de la materia:
| Propiedad |
Estado |
Estado líquido |
Estado gaseoso |
Estado plasmático |
|---|---|---|---|---|
| Tipo de materia | Materia fija | Fluidos con viscosidad | Gases | Gases calientes (con carga eléctrica) |
| Atracción entre partículas |
Alta | Intermedia | Baja | Baja |
| Movilidad de partículas |
Baja | Intermedia | Alta | Alta |
| Volumen | Con volumen | Con volumen | Sin volumen | Sin volumen |
| Forma | Definida | Indefinida | Indefinida | Indefinida |
| Ejemplo | Piedras | Agua | Vapor de agua | TV de plasma |
Ver también Qué es la Materia
Estado sólido

El estado sólido es aquel que percibimos como materia fija, la cual se resiste a los cambios de forma y volumen. En la materia en estado sólido, las partículas tienen mayor atracción entre ellas, lo que reduce su movimiento y las posibilidades de interacción.
Algunos ejemplos de materia en estado sólido: rocas, madera, utensilios de metal, vidrio, hielo, grafito, ropa y granos de café.
Las características del estado sólido son:
- La fuerza de atracción entre las partículas individuales es mayor que la energía que causa separación.
- Es el estado en el que se necesita mayor cantidad de fuerza externa para separar las partículas.
- Las partículas se encierran en su posición limitando su energía vibracional.
- Mantiene su forma y volumen.
Saber más sobre Estado sólido
Estado líquido

El estado líquido corresponde a los fluidos cuyo volumen es constante, pero se adapta a la forma de su contenedor. Pueden tener un nivel de viscosidad variable, dependiendo de los elementos en los que se compone el líquido.
Algunos ejemplos de materia en estado líquido son: agua, bebidas refrigerantes, lava, mercurio a temperatura ambiente, aceite y saliva.
Las características del estado líquido son:
- Las partículas se atraen entre sí, pero la distancia es mayor que en los sólidos.
- Las partículas son más dinámicas que los sólidos, pero más estables que los gases.
- Tiene un volumen constante.
- Su forma es indefinida. Por ende, el líquido toma la forma de su contenedor.
Ver también: Estado líquido
Estado gaseoso

El estado gaseoso corresponde a los gases. Técnicamente se define como el agrupamiento de partículas con poca atracción entre sí que, al chocar unas con otras, se expanden en el espacio.
Algunos ejemplos de materia en estado gaseoso son: vapor de agua, oxígeno (O2), helio (He), el aroma de los perfumes, humo, el aire atmosférico y gas natural.
Las características del estado gaseoso son:
- La concentración de partículas en un mismo espacio es menor que la de los sólidos y los líquidos.
- Las partículas tienen poca atracción entre sí.
- Las partículas se encuentran en expansión, por lo cual son más dinámicas que los sólidos y los gases.
- No tiene forma ni volumen definido.
Ver también: Estado gaseoso
Estado plasmático

El estado plasmático es un estado semejante al gaseoso, pero posee partículas cargadas eléctricamente, es decir, ionizadas. Se trata, pues, de gases calientes.
La materia en estado plasmático es muy común en el espacio sideral y constituye, de hecho, el 99% de su materia observable. Sin embargo, el estado plasmático también se reproduce naturalmente en algunos fenómenos terrestres. Asimismo, se puede producir artificialmente para diversos usos.
Por ejemplo, hay plasma en el sol, las estrellas y las nebulosas. También está presente en las auroras polares, en los rayos y en el llamado Fuego de San Telmo. En cuanto a su producción artificial, algunos ejemplos son los televisores de plasma, los tubos fluorescentes y las lámparas de plasma.
Las características del estado plasmático son:
- Carece de forma y volumen definidos.
- Sus partículas están ionizadas.
- Carece de equilibrio electromagnético.
- Es buen conductor eléctrico.
- Forma filamentos, capas y rayos cuando se expone a un campo magnético.
Te puede interesar: Estado plasmático
Nuevos estados de la materia
En la actualidad, las investigaciones científicas han hallado nuevos estados de agregación de la materia mediante procedimientos artificiales. Los más conocidos están basados en la temperatura. Estos son el condensado de Bose-Einstein, el condensado fermiónico y el estado supersólido.
Sin embargo, se siguen estudiando otras teorías sobre posibles estados de la materia, como la molécula de Rydberg, el estado de Quantum Hall, la materia fotónica y el dropleton.
Condensado de Bose-Einstein (BEC)
El estado conocido como condensado de Bose-Einstein (BEC por sus siglas en inglés) se produce cuando determinados gases son sometidos a temperaturas cercanas al cero absoluto (-273.15°C). Llegado a este punto, alcanzan tal densidad y punto de congelación que los átomos no se pueden mover.
Se trata de un estado de la materia que se logró artificialmente en el año 1995. Desde entonces, también es conocido como el quinto estado de la materia.
Un ejemplo del BEC son los materiales con superconductividad, es decir, que pueden transmitir electricidad sin ejercer resistencia alguna y sin perder energía.
Las características del estado condensado de Bose-Einstein son:
- Sus partículas son bosones.
- Es observable solo a nivel subatómico.
- Presenta superconductividad (resistencia eléctrica nula).
- Su estado de energía mínimo se conoce como estado fundamental.
Profundiza en: Estado condensado de Bose-Einstein
Condensado de Fermi
El condensado de Fermi o condensado fermiónico es aquel donde la materia es superfluida, es decir, que no tiene ningún grado de viscosidad. El comportamiento del estado fermiónico es semejante a una onda más que a una partícula. Se relaciona con el estado de Bose-Einstein.
Las características del condensando fermiónico son:
- Sus partículas son fermiones (y no bosones).
- Se produce en temperaturas cercanas al cero absoluto.
- Su estabilidad perdura muy poco tiempo.
Supersólido
El supersólido es un estado en el que la materia se ordena en el espacio con las propiedades de un superfluido. Solo en 2017 se encontraron pruebas claras de su existencia. Todavía se encuentra en investigación, lo mismo que otros estados hipotéticos.
Cambios de estados de la materia
Los cambios de estados de la materia son procesos que permiten que la estructura espacial de la materia cambie de un estado a otro. Dependen de las variaciones en las condiciones ambientales como la temperatura y/o la presión.
Tomando en cuenta los estados fundamentales de materia, los cambios de estado de la materia son: solidificación, vaporización, fusión, sublimación, sublimación inversa, ionización y desionización.

- Fusión o derretimiento. Es el cambio del estado sólido al estado líquido. Se produce cuando el sólido se expone a temperaturas más elevadas que su punto de fusión. Ocurre porque las altas temperaturas a las que se somete el sólido hace que las partículas se separen más y se muevan con más facilidad.
- Solidificación. La solidificación es el cambio del estado líquido al estado sólido. Cuando la temperatura de un líquido desciende, las partículas comienzan a aproximarse entre sí y se reduce el movimiento entre ellas. Al llegar al punto de congelación, se convierten en materia sólida.
- Vaporización. La vaporización es el cambio del estado líquido al estado gaseoso. Ocurre cuando se eleva la temperatura hasta llegar al punto de ebullición, rompiendo la atracción entre las partículas. Esto ocasiona su separación y el aumento de su movimiento, dando lugar a un gas.
- Condensación. La condensación es el cambio del estado gaseoso al estado líquido. Al bajar la temperatura y/o subir la presión, las partículas del gas pierden alguna movilidad y se aproximan entre sí. Esta aproximación explica el paso del gas al líquido.
- Sublimación. La sublimación es el cambio del estado sólido al estado gaseoso sin pasar por el estado líquido. Se produce, por ejemplo, en las esferas de naftalina. Estas esferas que se usan para alejar las polillas de los armarios tienen la propiedad de evaporarse con el tiempo, sin entrar en un estado líquido.
- Sublimación inversa. Se llama sublimación inversa, sublimación regresiva, deposición o cristalización al cambio del estado gaseoso al sólido de manera directa. Lo que ocurre aquí es que un gas se solidifica de forma inmediata, sin entrar en un estado líquido.
- Ionización. La ionización es el cambio de gas a plasma, el cual se produce cuando las partículas del gas son cargadas eléctricamente. Esto es posible cuando se calienta un gas.
- Desionización. La desionización consiste en el paso del estado plasmático al estado gaseoso. Se trata, pues, del proceso contrario a la ionización.
A continuación, presentamos una tabla que resume los cambios de la materia y expone un ejemplo por cada uno.
| Proceso | Cambio de estado | Ejemplo |
|---|---|---|
| Fusión | Sólido a líquido. | Deshielos. |
|
Solidificación |
Líquido a sólido. | Agua a hielo. |
| Vaporización | Líquido a gaseoso. | Agua a vapor de agua. |
| Condensación | Gaseoso a líquido. | Lluvia. |
| Sublimación | Sólido a gaseoso. | Hielo seco. |
| Sublimación inversa | Gaseoso a sólido. | Vapor de agua a nieve. |
| Ionización | Gaseoso a plasmático. | Letreros de neón. |
| Desionización | Plasmático a gaseoso. | El humo que resulta al apagar una llama. |
Te puede interesar:
- Cambios de estado de la materia
- Propiedades de la materia
- Propiedades intensivas y extensivas de la materia
- Qué es la antimateria
Cómo citar: Significados, Equipo (25/08/2025). "Estados de la materia". En: Significados.com. Disponible en: https://www.significados.com/estados-de-la-materia/ Consultado:











