Cambios de estado de la materia
Los cambios de estado de la materia se refieren a las transformaciones que sufre la materia de un estado al otro sin cambiar su composición. Estos cambios se producen cuando varía la presión y/o la temperatura.
En la Tierra, se manifiestan de forma natural los estados sólido, líquido, gaseoso y plasmático. Los cambios de estado que se dan entre estos son: vaporización, fusión, solidificación, sublimación, sublimación inversa, ionización y desionización.
Veamos en qué consisten, cómo se producen y cuáles son los ejemplos más comunes en la vida diaria.
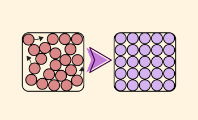
Solidificación (líquido a sólido)

La solidificación es el cambio del estado líquido al sólido. Se produce cuando desciende sensiblemente la temperatura de un líquido o fluido.
¿Cómo ocurre la solidificación? Cuando la temperatura del fluido desciende, las partículas se van aproximando unas a otras cada vez más, hasta quedar tan compactas que se reduce el movimiento entre ellas. Esta aproximación y falta de movilidad entre las partículas es lo que le da firmeza a los sólidos.
El punto máximo en el cual el fluido se endurece se conoce como punto de congelación.
Ejemplos de solidificación:
- Formación de hielo.
- Endurecimiento del chocolate.
- Endurecimiento de metales fundidos (joyas, herramientas de trabajo, etc.).
- Fabricación de jabones en pastilla.
- Endurecimiento de la gelatina.
Vea también Solidificación.
Fusión o derretimiento (sólido a líquido)

La fusión o derretimiento es el cambio del estado sólido al líquido. La fusión ocurre cuando el sólido se encuentra expuesto al aumento de la temperatura.
¿Cómo ocurre la fusión o el derretimiento? Cuando se eleva la temperatura de manera considerable, las partículas de la materia sólida comienzan a separarse unas de otras. A medida que la separación es mayor, las partículas ganan más movimiento. En consecuencia, la materia empieza a ganar un aspecto fluido y pierde su forma. Es decir, el sólido se convierte en líquido.
Ejemplos de fusión:
- Deshielo de los casquetes polares.
- Chocolate fundido.
- Mantequilla derretida para cocinar.
- Cera de vela derretida (parafina).
- Derretimiento de helados en paleta expuestos al calor del ambiente.
Ver también:
Vaporización o evaporación (líquido a gaseoso)

La vaporización es el cambio del estado líquido al gaseoso. Esto ocurre cuando un líquido es expuesto a una elevación de la temperatura.
¿Cómo ocurre la vaporización? La vaporización es un proceso que avanza constante y lentamente en ciertos fluidos, pero se acelera cuando el líquido alcanza el punto de ebullición.
En dichas condiciones, las partículas empiezan a alejarse unas de otras. La interacción entre ellas se rompe y, por ende, su movimiento se hace expansivo, dando lugar a la formación del estado gaseoso.
Ejemplos vaporización:
- Vapor de agua hirviendo.
- Secado de un piso húmedo.
- Evaporación del sudor.
- Secado de la ropa al aire libre.
- Formación de nubes por evaporación del agua terrestre.
Te puede interesar: Evaporación.
Condensación (gaseoso a líquido)

La condensación es el cambio del estado gaseoso al líquido. La condensación ocurre cuando baja la temperatura y/o sube la presión en el ambiente.
¿Cómo ocurre la condensación? Cuando la temperatura desciende y/o la presión sube, las partículas que conforman el gas comienzan a acercarse unas a otras, de modo que pierden parte de su movilidad. De este modo se produce el cambio del estado gaseoso al líquido.
Ejemplos de condensación:
- La lluvia.
- La transpiración de un vaso con líquido frío.
- El rocío.
- Empañado de vidrios y espejos.
Vea también Condensación.
Sublimación (sólido a gaseoso)

La sublimación es el cambio directo del estado sólido al gaseoso. En este caso, no hay paso por el estado líquido. De hecho, la palabra sublimación proviene del latín sublimare, que significa ‘elevarse’.
La sublimación se produce cuando un sólido conservado a una temperatura extremadamente baja entra en contacto con una temperatura mayor, dentro de una presión determinada.
¿Cómo se produce la sublimación? Para todas las sustancias existe un punto de temperatura y presión en que el estado sólido, el líquido y el gaseoso coexisten en equilibrio, el cual se llama punto triple.
Cuando la temperatura del estado sólido se encuentra por debajo del punto triple y, además, la presión de vapor es lo suficientemente baja, no existen condiciones para la formación de líquido. Entonces, cualquier aporte de energía (calor), por pequeño que sea, provoca que las partículas del sólido se separen abruptamente y se expandan en el espacio en forma de gas.
Por ejemplo, el hielo seco es un bloque sólido de dióxido de carbono (CO2) y se conserva a una temperatura de -78 °C, es decir, por debajo del punto triple. Cuando el hielo seco se expone a la temperatura del ambiente, a una presión inferior de 5.2 atmósferas, se transforma en gas directamente. Esto es sublimación.
Ejemplos de sublimación:
- Sublimación de hielo seco.
- Sublimación de naftalina.
- Sublimación de tinta solidificada.
- Sublimación química para medicamentos.
Vea también Sublimación.
Sublimación inversa o deposición (gaseoso a sólido)

La sublimación inversa consiste en el cambio directo del estado gaseoso al sólido. La sublimación inversa se conoce también como deposición, sublimación inversa, sublimación regresiva, desublimación o cristalización.
La deposición o sublimación inversa ocurre cuando el gas entra en contacto con temperaturas muy bajas de manera rápida o repentina.
¿Cómo se produce la sublimación inversa o deposición? Cuando un gas o vapor es expuesto a muy bajas temperaturas y en ciertas condiciones de presión, pierde su energía calórica velozmente. Así, se compactan sus partículas, y pasa al estado sólido.
Ejemplos de sublimación inversa:
- Nieve.
- Formación de escarcha.
- Estelas de los aviones en el cielo.
- Formación de hollín en las chimeneas.
Ionización (gaseoso a plasmático)

La ionización es el cambio de gas a plasma. Este proceso tiene lugar cuando un gas se calienta.
¿Cómo se produce la ionización? Al calentarse el gas, las partículas que componen el gas comienzan a moverse más rápidamente y chocan entre sí. Esto aumenta el nivel de energía, provocando que los electrones más externos de los átomos se pierdan. A raíz de esto, los átomos se convierten en iones.
Parte de la energía de estos átomos y de los electrones puede dar lugar a fotones. Este proceso hace que el gas brille, lo que da lugar al plasma.
Ejemplos de ionización:
- Los rayos de las tormentas eléctricas.
- Las auroras polares (aurora boreal y aurora austral).
- Luces de neón.
- Televisores de plasma.
- Lámparas de plasma.
Desionización (plasmático a gaseoso)

La ionización es el cambio de gas a plasma. Se trata del proceso inverso a la ionización. Se produce cuando un gas cargado eléctricamente se enfría.
¿Cómo se produce la desionización? Al contrario de la ionización, la desionización es un proceso en el cual un gas se enfría, lo que hace que pierda su carga energética. Los átomos dejan de ser iones y, por lo tanto, el gas deja de generar fotones.
Ejemplo de desionización:
- El humo que se genera durante el proceso de soldadura del metal.
- El humo de una llama recién apagada.
Te puede interesar:
Cómo citar: (05/09/2023). "Cambios de estado de la materia". En: Significados.com. Disponible en: https://www.significados.com/cambios-de-estado-de-la-materia/ Consultado: