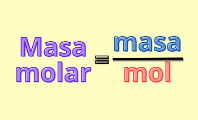Mol (Química)
Un mol es la unidad que expresa la cantidad de una sustancia en el Sistema Internacional (SI). Un mol equivale a 6,022 x 1023 unidades elementales, es decir, a dicha cantidad de átomos, partículas o moléculas. Este valor es también una constante, llamada número o constante de Avogadro.
Por ejemplo:
- Un mol de átomos de hidrógeno contiene 6,022 x 1023 átomos de hidrógeno.
- Un mol de agua (H2O) contiene 6,022 x 1023 moléculas de agua.
- Un mol de electrones es igual a 6,022 x 1023 electrones.
Un mol contiene un número fijo de elementos, así como una docena siempre tiene 12 elementos. Por ejemplo, cuando hablamos de una docena de huevos, sabemos que son 12 huevos; si fuera un mol de huevos, entonces tendríamos 6,022 x 1023 huevos.
El concepto de mol en química fue actualizado por el Comité Internacional para los Pesos y Medidas en 2019. La definición anterior de mol era "la cantidad de sustancia de un sistema que contiene tantas entidades elementales como átomos en 12 gramos de carbono 12".
La masa de un mol es lo que se conoce como masa molar. Así, cada mol de un elemento químico, molécula o partícula tiene una masa determinada. Por ejemplo, 1 mol de hidrógeno tendrá una masa de 1,008 gramos, mientras 1 mol de oro tiene una masa de 196,96657 gramos.
Fórmula para calcular moles
Para calcular los moles de una sustancia cuya masa es conocida, basta con utilizar la siguiente fórmula:
En que:
- n es el número de moles (mol);
- m es la masa de la sustancia, en gramos (g);
- M es la masa molar o molecular de la sustancia, en gramos sobre mol (g/mol) o kilogramos sobre mol (kg/mol).
Con masa molar o molecular (M), nos referimos a aquella masa de la sustancia, sea de un elemento o molécula, que hay en 1 mol de dicha sustancia.
Ejemplos del cálculo de moles
Vamos a retomar los ejemplos del hidrógeno (H) y oro (Au). En primer lugar, 1 mol de hidrógeno tiene una masa aproximada de 1,008 gramos. Si tenemos 5 gramos de hidrógeno, podemos determinar el número de moles usando la fórmula:
En 5 gramos de hidrógeno hay 4,96 moles. En segundo lugar, 1 mol de oro equivale a unos 196,967 gramos. Aplicamos otra vez la fórmula para saber cuántos moles de oro hay en 2 kilogramos o 2000 gramos:
Por tanto, en 2 kilogramos de oro hay 10,15 moles.
Para ambos valores, podemos convertir el número de moles en cantidad de unidades elementales utilizando una simple regla de tres. Te lo mostramos aprovechando los valores obtenidos para el hidrógeno y oro:
Vea también Número de Avogadro, Molécula, Átomo y Estequiometría.
Referencias
BIPM, The International System of Units (2019) SI Brochure-Mise en pratique for the definition of the mole in the SI. Appendix 2. 9.ed.
Bindel, T.H. (2021) Introducing High School Students to the Avogadro Number and the Mole Concept Using Discovery with Calculations Based on physical properties of elements, crystal Structures, and 28Si Spheres. J.Chemical Education 98: 790-795
Cómo citar: Fernandes, Ana (29/10/2025). "Mol (Química)". En: Significados.com. Disponible en: https://www.significados.com/mol/ Consultado: